DNA Marker DS15000+2000(M1241-M1242)

DNA Marker DS15000+2000(M1241-M1242)
M1241,60次
M1242,60次×3
品牌:东盛
DSTM15000+2000
M1241/M1242
60次/60次×3
建议上样量
3-5 µl/次。可根据上样孔大小选择合适上样量。
DSTM15000+2000已预混上样缓冲液,可直接进行电泳分析。
建议电泳条件
8 cm 1 %琼脂糖凝胶,
1×TAE,7 V/cm,45min。
保存
常温保存3个月,长期保存请置于-20℃。
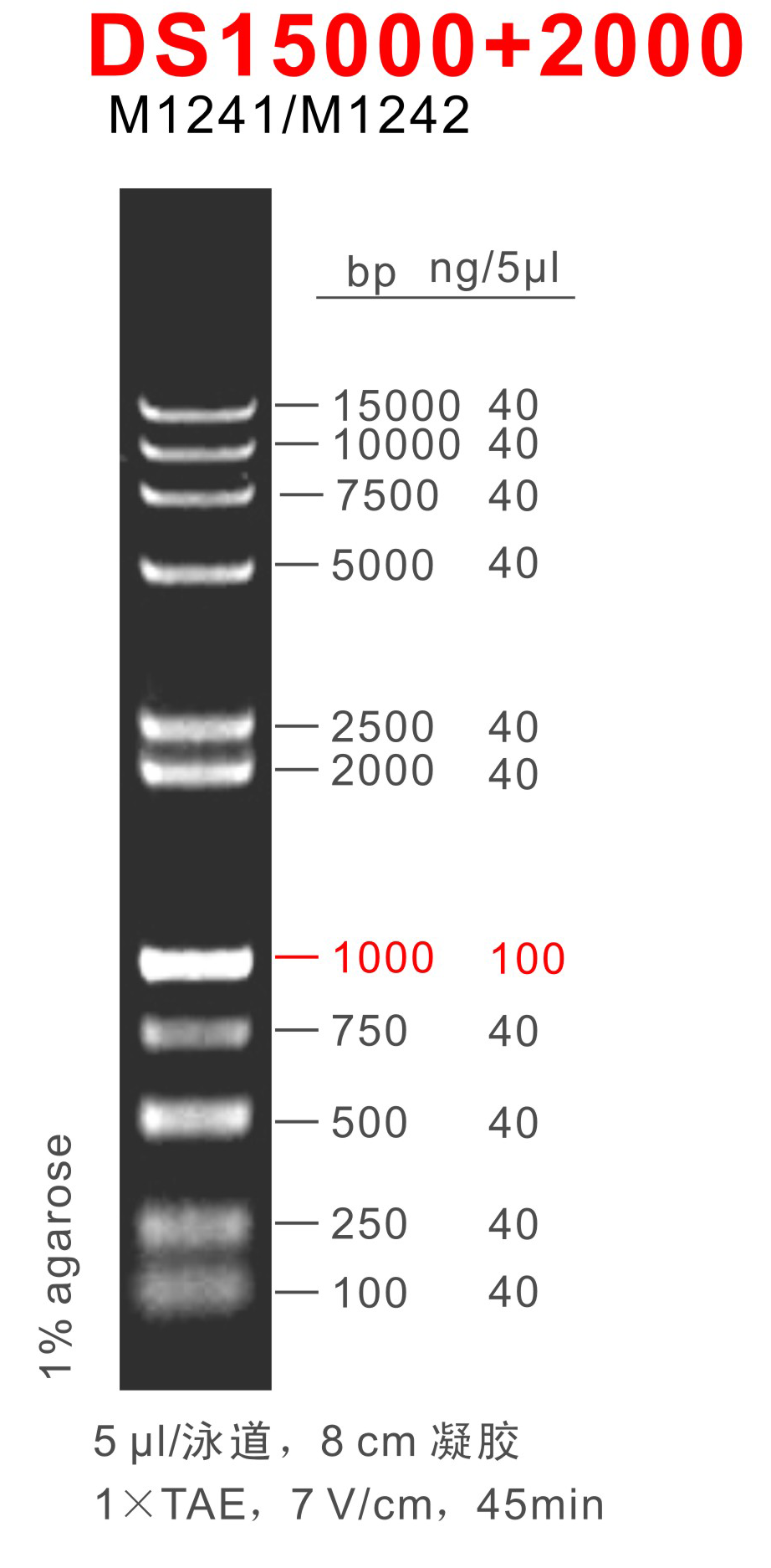
各条带含量
指示带 100 ng/5µl
非指示带 40 ng/5µl
产品说明
DSTM15000+2000由11条双链线状DNA片段混合而成,适用于确定100 bp至15 kb的线性双链DNA片段大小,指示带为1000 bp,便于电泳后观察。每条带都通过严格的物理定量,可用于测定目的片段的大小和含量。
产品浓度为100 ng/µl。
条带组成(bp)
100、250、500、750、1,000、2,000、2,500、5,000、7,500、10,000、15,000
注意事项
● 请选择高品质的琼脂糖,并及时更换电泳缓冲液。溶胶不充分会导致因胶浓度不均而出现电泳条带异常;陈旧的缓冲液离子缓冲能力不足,可能导致Marker条带泳动缓慢,并伴随弥散现象。
● 胶浓度、电压、电泳时间是影响DNA片段分离的主要因素,为获得最佳电泳分离效果,建议按照东盛推荐的条件进行电泳分析。
● 上样量的多少取决于样品的浓度与加样孔的大小。由于东盛Marker的浓度较高,通常对于宽3mm(厚0.75-1mm)的加样孔,建议上样2-3 μl,对于宽5mm(厚0.75-1.5mm)的加样孔,建议上样4-6 μl。过多的上样量可能导致条带相互挤压,分散不充分,跑不开,影响条带分离效果。
● 使用本产品进行定量分析时,可将目的片段做梯度上样,选择亮度与Marker条带最为接近的片段进行分析。
● 进行PAGE胶电泳分析时,建议取0.5-1 μl Marker并用1×loading buffer稀释到适当体积上样。
Q&A
● 对于非变性凝胶电泳,Marker是否需要DNA变性?
答:本公司Marker产品中只有Lambda DNA Marker为质粒酶切产物,在电泳上样前如加热处理可获得最佳效果,其余产品均不需点样前加热处理;另外电压太高也会使凝胶过热和DNA变性造成带型异常。
● 当DNA停留在凝胶点样孔处时该怎么办?
答:检查胶浓度是否在适合分离DNA片段的范围,点样孔是否高质,确保电泳的正负极正确,检查电泳缓冲液是否具有缓冲能力,确保DNA样品的纯度,如进行PCR产物的纯化,确保样本中没有或只存在少量的DNA结合蛋白或其他可与DNA结合的化合物。
● 为什么DNA条带不理想?
答:影响电泳条带的因素很多,如凝胶种类或浓度不合适,质量不佳;上样量过多或过少;样本的纯度不高,盐浓度过高;电泳缓冲液缓冲能力不足,有核酸酶污染;电泳条件不正确;染色不充分或不均匀;跑胶后没有及时拍照。
● 为什么定量数据不正确以及如何准确定量样品?
答:样品和Marker的上样条件不同,参考条带不正确,凝胶的不均匀染色或背景过高都会干扰凝胶定量结果。样品DNA和Marker DNA在电泳前选用相同的上样染料处理,调整样品浓度,使其在凝胶中的含量与分子量最接近标准DNA条带,样品DNA和Marker的上样体积尽量接近,样品用1×上样缓冲液稀释;定量时以分子量最接近的标准条带为参照物,分析样品条带的含量;利用凝胶图像分析软件,如SensiAnsys可对DNA进行准确定量,比目测条带方法更精确。
● 为什么在变性聚丙烯酰胺/尿素凝胶里电泳时会出现杂带?
答:一般来说,双链DNA Marker不推荐用于变性电泳,否则会产生非正常带型,即出现所谓的杂带。这种出现异型带的现象,在100 bp以下的条带极易发生。当您的实验不可避免的要使用变性聚丙烯酰胺/尿素凝胶进行电泳时,我们建议,将样品和Marker选用同样的变性上样缓冲液进行变性处理后上样,以消除二级结构。