外泌体介绍及提取方法
外泌体介绍及提取方法
背景介绍:
刚发现外泌体时,这种比多泡体还要小的细胞外囊泡被视为细胞外排出的代谢垃圾,但随着对这种细胞外囊泡不断地深入研究,发现这种细胞外囊泡在细胞之间的通讯交流中发挥着极其重要的作用。
外泌体是什么?
外泌体是机体所有活细胞分泌的一种直径约为30-150nm的细胞外囊泡,广泛存在于各种生物体液(血液、尿液、母乳、唾液、胸水、腹水、脑脊液等)中。它们由蛋白质、脂质、核酸的特定成分组成,可以将信号传递给受体细胞,从而介导细胞间的通讯。外泌体在多种生物学功能中发挥着重要作用,包括参与RNA、蛋白质、酶和脂质等生物分子的转移,以及各种生理和病理过程的调节。
外泌体属于细胞外囊泡的一种,根据直径大小以及释放机制的不同可将细胞外囊泡主要分为外泌体、微囊泡、凋亡小体,它们都参与细胞间信息传递,但目前对于外泌体的研究最多。
表 外泌体与其他细胞外囊泡的区别
分类 | 外泌体 | 微囊泡 | 凋亡小体 |
直径 | 30-150nm | 100-1000nm | 500-4000nm |
密度 | 1.1-1.18g/mL | 1.02-1.22g/mL | 1.16-1.28g/mL |
来源 | 细胞内的多泡小体与细胞膜融合后,其内的小泡释放到细胞外 | 细胞膜出芽形成 | 凋亡时细胞膜皱缩内陷,分割包裹胞质形成的泡状小体 |
内含物 | mRNA、miRNA、非编码RNA、蛋白(细胞质、膜)、MHC | mRNA、miRNA、非编码RNA、蛋白 | 核组分、DNA、细胞器 |
蛋白标志物 | Alix、TSG101、HSC70、CD63、CD81、CD9 | Selectin、integrins、CD40、MMP | Histones |
功能 | 细胞内通讯、细胞间物质交流 | 细胞内通讯、在细胞间运输遗传物质 | 调节病理和生理过程 |
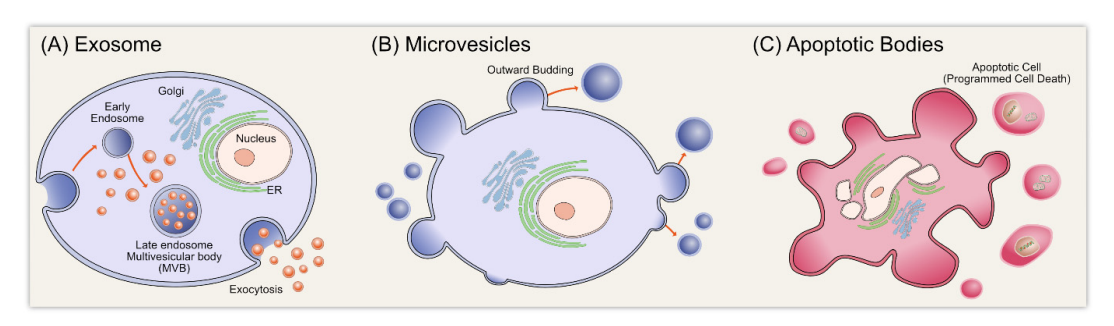
图 外泌体与其他细胞外囊泡
外泌体的结构组成:
外泌体具有脂质双分子层结构,由胆固醇、鞘磷脂和磷酸甘油酯等成分共同组成,在其脂质双分子层的表面附着有粘附分子、主要组织相容性复合体(major histocompatibility complex,MHC)、大量的特定蛋白质,包括四跨膜蛋白、热休克蛋白等等和各种特定的配体(CD9、CD63、CD81等)。在外泌体的内腔中还携带各种生物活性物质,包括核酸、某些酶类、蛋白分子、细胞代谢物等,核酸例如信使核糖核酸(messenger ribonucleic acid,mRNA)、微小核糖核酸(micro ribonucleic acid,miRNA)、脱氧核糖核酸(Deoxyribonucleic acid,DNA)和长链非编码核糖核酸(Longnon-coding ribonucleic acid,LncRNA)等。
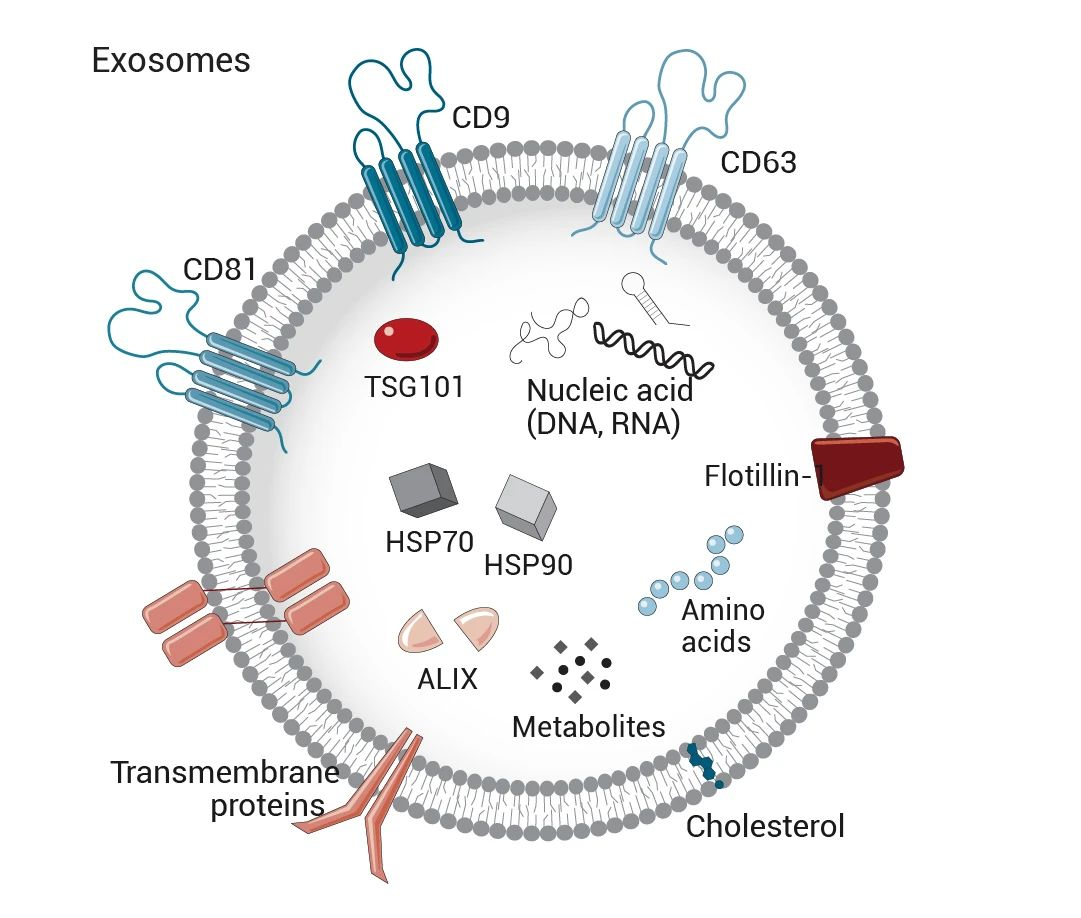
图 外泌体的结构组成
外泌体的功能:
外泌体的功能起决于其所来源的细胞类型。外泌体能够将核酸、蛋白质和脂质在内的多种生物活性分子从供体细胞转移到受体细胞,介导细胞间通讯和分子转运;并且外泌体可以由所有类型的活细胞分泌,在体液中广泛分布。它可参与机体免疫应答、抗原提呈、细胞迁移、细胞分化、细胞迁移、肿瘤侵袭等方面,因此外泌体在生理病理标志物和药物递送方面有巨大的应用潜力。
外泌体提取:
进行外泌体研究,首先要将其从样本中提取出来。目前已有许多基于外泌体物理及生化特性的分离方法,传统方法包括超速离心、密度梯度离心、超滤、尺寸排阻色谱(size-exclusionchromatography,SEC)、聚合物沉淀法、免疫亲和层析,还有一些新的微流体技术、商业试剂盒。
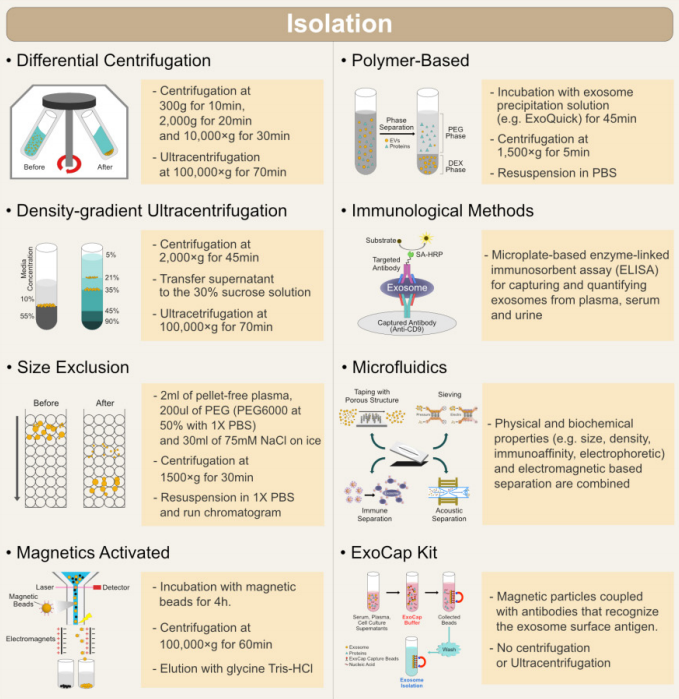
图 外泌体分离纯化方法合集
超速离心:
超速离心法是最常用也是分离外泌体的“金标准”方法。其原理是利用溶液颗粒大小和密度导致沉降速率不同,来分离不同组分。该方法包含以下步骤:低速离心去除细胞和凋亡碎片;其次以更高离心力消除更大囊泡;最后高速离心沉淀外泌体。该方法操作简便,可以扩展为大规模外泌体制备。在过去30年中,超速离心法被广泛应用于从细胞培养基、血清、体液中分离外泌体。但是该方法特异性不强、可混有分子量相近的蛋白质,同时高速离心力可能破坏外泌体膜泡影响下游分析。
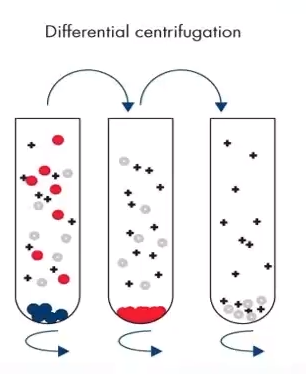
图 超速离心法分离外泌体
密度梯度离心:
密度梯度离心利用颗粒大小与密度差异对外泌体进行分离。密度梯度离心会预先使用蔗糖或碘克沙醇制作密度梯度。样品从顶部加入离心管,在离心过程中逐渐自上而下沉降,在一定密度区间聚集。外泌体通常密度范围为1.1~1.2g/mL。该方法的局限性是分离样本容量受到密度区带宽度的限制,因此密度梯度离心不便于处理大样本。
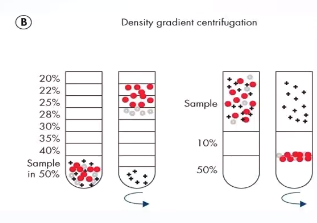
图 密度梯度离心分离外泌体
超滤:
超滤是基于外泌体尺寸进行分离的方法。根据膜孔的尺寸和截留分子量,将小颗粒通过膜孔进入滤液,大颗粒截留在膜表面。超滤的主要缺点为液体流动方向平行膜孔方向,造成大颗粒堵塞膜孔,同时产生的剪切力也会使外泌体变形或裂解。
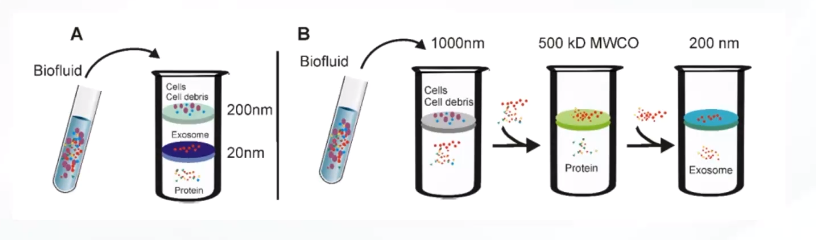
图 超滤法纯化外泌体
尺寸排阻色谱(SEC):
SEC原理为根据颗粒尺寸进行分离。在色谱柱中填充多孔固定相,小颗粒可以穿过固定相中的空隙,因此沉降路径变长,较大颗粒更晚沉降,因此可以分离尺寸差别较大的颗粒。通常SEC会先进行超速离心预处理以此减少杂质、提高纯度。SEC最大的优势是可以很好的保留外泌体活性。
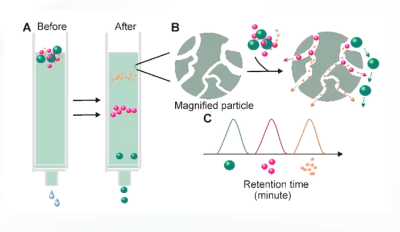
图 尺寸排阻色谱(SEC)纯化外泌体
聚合物沉淀法:
聚合物沉淀原理是利用超亲水聚合物,如PEG结合溶液中水分子使溶质溶解度降低进而沉淀析出,最后通过低速离心获得外泌体。可以广泛用于各种样品类型,如血液、培养基、尿液、脑脊液等。其优点是可处理大样本,产量较高。缺点是分离的外泌体会受到其他蛋白质污染。

图 聚合物沉淀法纯化外泌体
免疫亲和层析:
免疫亲和层析基本原理通过配体与抗体特异结合进而分离纯化。一般用外泌体表面生物标记物作为配体,如四跨膜蛋白超家族、囊泡转运分类内涵体复合物、复合物相关蛋白。抗体吸附在磁珠、多孔二氧化硅单片板、膜亲和过滤器上,溶液通过时可特异结合外泌体表面蛋白进行分离纯化。常见方法有基于微孔板的酶联免疫吸附测定与磁珠免疫捕获。此类方法具有高特异性,并可以保证外泌体生物活性。
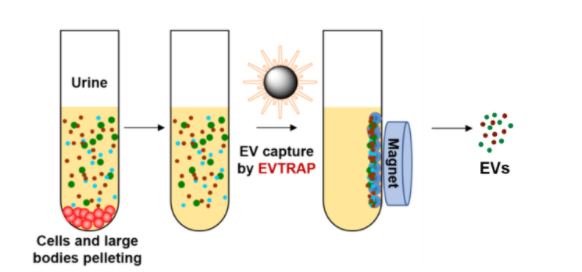
图 磁珠法免疫捕获外泌体
相关外泌体产品链接:https://www.noninbio.com/search/site.html?kw=%E5%A4%96%E6%B3%8C%E4%BD%93&syi=6825&tabs=1